・内部エネルギーとは
・内部エネルギーの公式
・熱力学第一法則とは
内部エネルギーについては、物理基礎でも解説をしました。
物理基礎での説明とほぼ同じになってしまいますが、改めて内部エネルギーとは何かについて、わかりやすく簡単に解説していきます。
内部エネルギーとは
”]
分子のもつ運動エネルギー+位置エネルギーのこと
単原子分子理想気体では、
$$U=\frac{3}{2}nRT$$
単原子分子理想気体かつ、物質量n[mol]が一定の場合
$$ΔU=\frac{3}{2}nRΔT$$
内部エネルギーとは、分子のもつ運動エネルギー+位置エネルギーのことです。
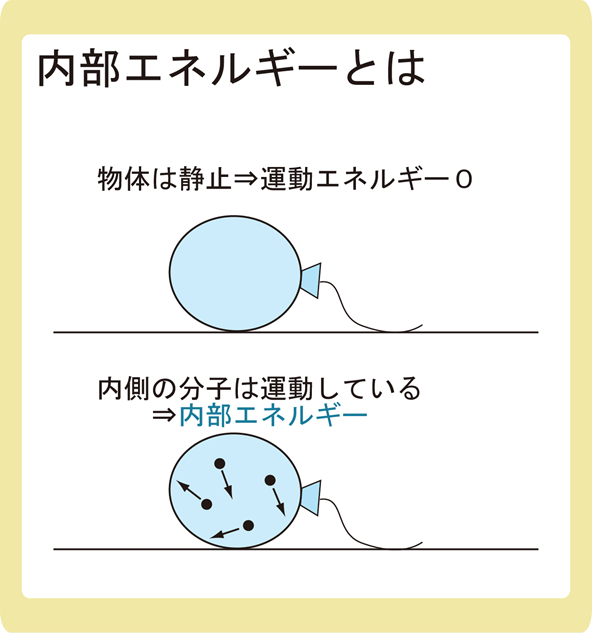
上図のように風船が静止しているとき、物体のもつ運動エネルギーは0Jなのですが、風船の内側にある分子は運動エネルギーを持っているはずですよね。
このような、気体分子の持っているエネルギーのことを内部エネルギーといいます。
理想気体では分子間力がはたらかないと考えているため、位置エネルギーは0Jであると考えます。
単原子分子理想気体であるとき、分子1個が持つ気体分子の運動エネルギーは
$$\frac{1}{2}m\overline{v^2}=\frac{3}{2}\frac{R}{N_A}T$$
でした。
分子がNA個集まって1molなので、分子がn[mol]の場合は両辺にnNAをかければよいので、
$$nN_A×\frac{1}{2}m\overline{v^2}= nN_A ×\frac{3}{2}\frac{R}{N_A}T\\
U=\frac{3}{2}nRT$$
となり、これが内部エネルギーであると考えることができます。
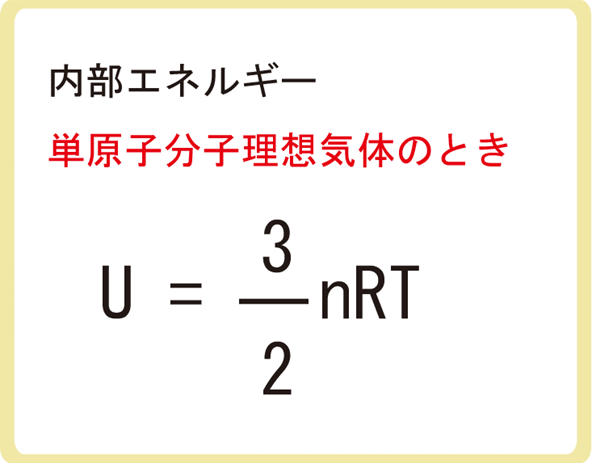
ここで大事なのは、\(U=\frac{3}{2}nRT\)は単原子分子理想気体のときしか使うことができない点です。
何でもいいので物理の問題集を開いてみてください。問題文に「単原子分子理想気体のとき」と書いてある問題と書いていない問題、大雑把に半々くらいに分かれていますよね?
問題文に「単原子分子理想気体のとき」と書かれている場合、ほぼ確実に\(U=\frac{3}{2}nRT\)を使う問題であるため、必ずチェックしておきましょう。
なお、物質量n[mol]が一定の場合は、\(ΔU=\frac{3}{2}nRΔT\)とすることができます。
熱力学第一法則とよく一緒に使うため、こちらの公式も覚えておくと良いでしょう。
熱力学第一法則とは
気体の内部エネルギーは、熱を受け取るか仕事をされると増加する
$$ΔU=Q+W$$
$$Q=ΔU+W’$$
(ΔU:内部エネルギーの変化量[J] Q:気体に与えた熱量[J] W:気体にされた仕事[J] W:気体がした仕事[J])
熱力学第一法則とは、気体の内部エネルギーは、熱を受け取るか仕事をされると増加することであり、要は、エネルギーは保存するという法則です。
物理基礎で行った説明とほぼ同じ説明になってしまいますが、改めて確認していきましょう。
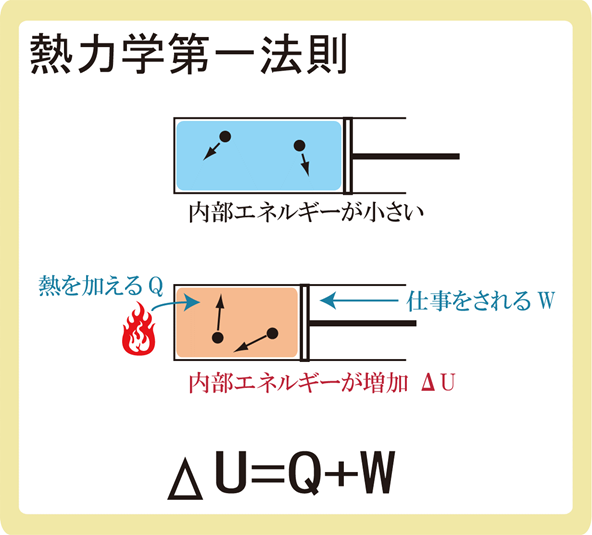
Uは内部エネルギーであり、ΔUになると内部エネルギーの変化量です。
この法則は気体だけではなく固体や液体でも成立するのですが、高校物理基礎・物理では気体の話しか出てこないので、ここでは気体という前提で説明をします。
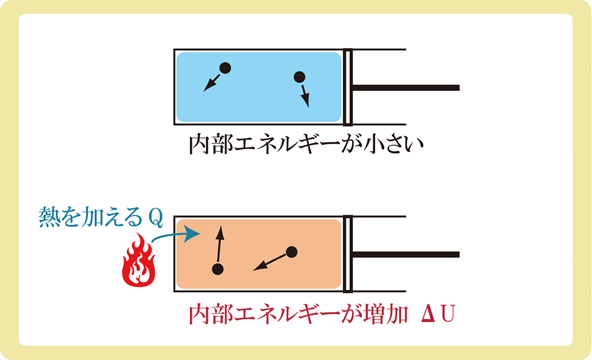
まず、気体に熱Qを与えると内部エネルギーは増加します。
内部エネルギーが増加するとは、大雑把に言うと気体分子の運動が早くなるということです。
これはとてもイメージしやすいですね。
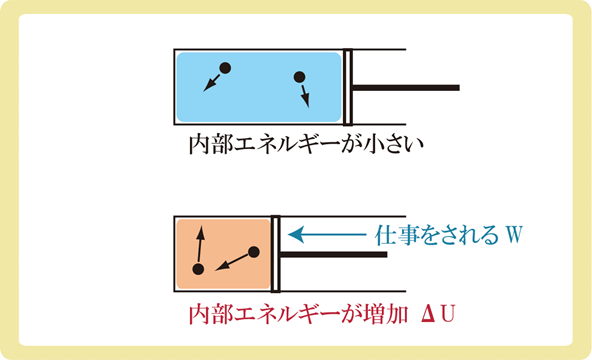
同様に、気体に仕事がされる場合も内部エネルギーが増加します。
そもそも、仕事とはエネルギーを与えることなので、仕事がされるとエネルギーが増えて当然です。
なお、気体が仕事をされると気体は圧縮し、気体が仕事をすると気体は膨張します。
熱力学第一法則の公式はどっち?
熱力学第一法則の公式は
$$ΔU=Q+W$$
$$Q=ΔU+W’$$
の2種類が存在しています。
この2つの公式の違いは、気体がされた仕事Wと気体がした仕事W’を使い分けている点です。
気体がされた仕事Wと気体がした仕事W’には
$$W=-W’$$
という関係があります。
これを使うことで
$$ΔU=Q+W\\
ΔU=Q-W’\\
Q=ΔU+W’$$
と式変形をすることができるのです。
問題集や参考書によっては、2つの式を使い分けるという説明もあるのですが、
$$ΔU=Q+W$$
の方の公式のみを使って下さい。
中途半端に使い分けるよりも、片方のみを使い続ける方が変なミスをしなくなるので、気体がした仕事W’は気体がされた仕事Wに変えてしまいましょう。
まとめ
内部エネルギーとは分子のもつ運動エネルギー+位置エネルギーのことで、単原子分子理想気体のときは\(U=\frac{3}{2}nRT\)となります。
単原子分子理想気体の場合は、まず間違いなく\(U=\frac{3}{2}nRT\)を使うと思ってください。
熱力学第一法則は\(ΔU=Q+W\)です。このとき、Wは気体がされた仕事であるため、気体が仕事をされた(圧縮された)のか、気体が仕事をした(膨張した)のかを確認する必要があります。












